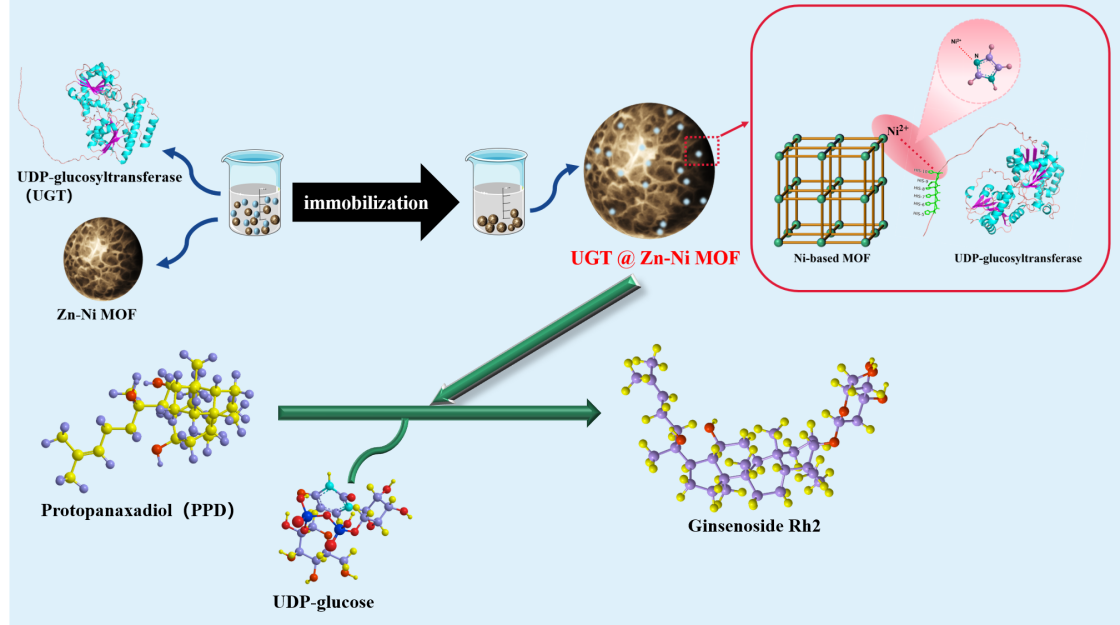
近日,我院武占省教授課題組劉嘯塵博士指導(dǎo)研究生在國際期刊《ACS Applied Materials & Interfaces》(中國科學(xué)院2區(qū)Top,IF=9.5)上發(fā)表題為“One-step purification and immobilization of glycosyltransferase with Zn-Ni MOF for the synthesis of rare ginsenoside Rh2”(DOI:10.1021/acsami.3c18928)的研究工作,該工作提出使用溶劑熱法制備的雙金屬Zn-Ni MOF對帶有His標(biāo)簽的糖基轉(zhuǎn)移酶具有優(yōu)異的特異性吸附性能,能夠?qū)崿F(xiàn)酶的一步純化和固定化,并且固定化酶在稀有人參皂苷Rh2的催化合成中具有超高的穩(wěn)定性和循環(huán)使用性,大大的解決了游離酶在催化反應(yīng)中的受限問題。該論文第一作者為我院2021級碩士研究生李志燕,通訊作者為劉嘯塵導(dǎo)師、武占省教授,西安工程大學(xué)為第一和通訊單位。
傳統(tǒng)的固定化酶方法都存在一些缺陷,例如:酶在催化過程中容易脫落;使用交聯(lián)劑會(huì)導(dǎo)致酶活性喪失;需要高純度的酶,這大大增加了固定化過程的難度和成本。而利用過渡金屬離子與His標(biāo)簽酶上的咪唑基團(tuán)之間的金屬螯合作用,實(shí)現(xiàn)酶在金屬有機(jī)框架(MOF)中的特異性固定化,為解決這些難題提供了一種前景廣闊的方案。這種創(chuàng)新方法不僅提高了酶的穩(wěn)定性和重復(fù)使用性,還實(shí)現(xiàn)了酶的一步純化和固定化,有效避免了從粗酶溶液中純化酶的需要,從而大大節(jié)省了實(shí)驗(yàn)成本。在催化反應(yīng)中使用固定化酶對提高人參皂苷Rh2的轉(zhuǎn)化率具有巨大潛力。該研究制備的Zn-Ni MOF材料可作為帶有His標(biāo)簽酶的一步純化和固定化平臺(tái),為糖基轉(zhuǎn)移酶在稀有人參皂苷Rh2催化轉(zhuǎn)化中的實(shí)際應(yīng)用提供了新的思路。
本研究工作得到了國家重點(diǎn)研發(fā)計(jì)劃(2021YFC2101500)、國家自然科學(xué)基金(22008186)、陜西省高校青年科技創(chuàng)新團(tuán)隊(duì)(2022TD071)、陜西省自然科學(xué)基礎(chǔ)研究項(xiàng)目(2019JQ-523)的支持。(撰稿:劉嘯塵;審核:武占省)
文章鏈接:https://doi.org/10.1021/acsami.3c18928
